Zagadki chemiczne // Proszę o szklankę wody!
Nikt nie ma wątpliwości, że proszący ma na myśli wodę do picia. Związek o wzorze H2O czyli tlenek diwodoru, zawierający rozpuszczone w sobie gazy lub sole mineralne. I nawet chemik nie żądałby sprecyzowania terminu, choć wie dobrze, że nie każda woda to H2O . Ale mógłby- ot tak, z przekory – zaoferować szklankę jednej z 10 niżej podanych „wód”. Ale, że nierzadko wypicie jej mogłoby skończyć się tragicznie, sprawdźmy lepiej, czy aby na pewno dobrze wiemy, co to jest:
1. woda królewska
2. woda sodowa
3. woda utleniona
4. woda wapienna
5. woda ciężka
6. woda amoniakalna
Ad. 1
Woda królewska to mieszanina stężonego kwasu solnego i stężonego kwasu azotowego w stosunku objętościowym 3:1. Woda królewska rozpuszcza metale szlachetne, jak złoto i platynę, na które nie działa kwas azotowy. Z tej właściwości wody królewskiej skorzystał w czasie ostatniej wojny uczony duński Niels Bohr. Zmuszony nocą do ucieczki w Danii, wrzucił do butelki z wodą królewską swój złoty medal przyznany mu przez fundację Nobla; po powrocie do Danii zastał w laboratorium butelkę nietkniętą, wytrącił więc złoto i kazał ponownie odlać metal.
Rys. 1 Początek rozpuszczania się platynowej monety w wodzie królewskiej; kolby z wodą królewską
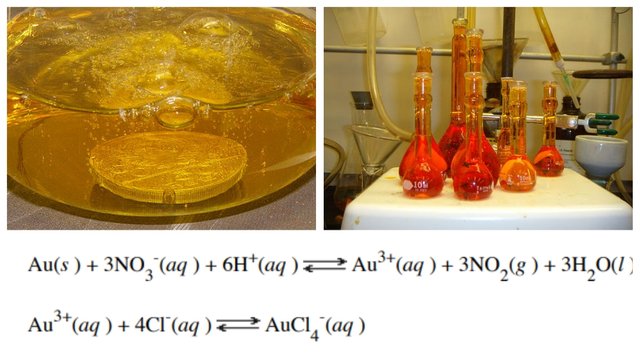
Woda królewska może rozpuszczać złoto dzięki swoim dwóm składowym kwasom, mających różne funkcje. Kwas azotowy jest mocnym utleniaczem. Jony chlorkowe, pochodzące z HCl tworzą kompleksy koordynacyjne z jonami złota, tym samym wydzielając je z roztworu.
Ad. 2
Woda sodowa jest roztworem kwasu węglowego H2CO3. Produkuje się ją nasycając wodę dwutlenkiem węgla pod ciśnieniem. „Wymyślił” ją Joseph Priestley, który również był odkrywcą tlenu.
Rys. 2 Joseph Priestley – angielski chemik, filozof i duchowny. Odkrywca m.in. amoniaku, tlenku węgla, chlorowodoru i kwasu siarkowego; bąbelki obecne w wodzie gazowanej; syfony, które umożliwiają saturację – czyli nasycenie wody gazem

Ad. 3
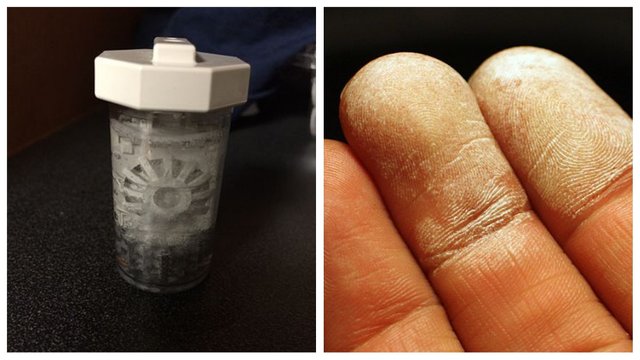
Woda utleniona to nazwa zwyczajowa 3% roztworu wodnego nadtlenku wodoru H2O2. Związek ten rozkłada się łatwo, wydzielając aktywny tlen – piana na wydzielającej się krwi to właśnie banieczki tlenu! Ma słabe własności bielące, ale można je łatwo polepszyć zwiększając stężenie nadtlenku wodoru do 30% – otrzymamy wtedy perhydrol. Używać się go do rozjaśniania włosów. Prawie całą produkcję nadtlenku wodoru używa się jako utleniacza paliw rakietowych jako że stężony roztwór jest środkiem wybuchowym.
Rys. 3 Roztwór wody utlenionej, w specjalnym pojemniku, pełniący funkcję płynu do soczewek- w czasie procesu dezynfekcjacji dochodzi do niszczenia osadów białkowych; palce, krótko po kontakcie z perhydrolem
Ad. 4
Woda wapienna to nasycony wodny roztwór wodorotlenku wapniowego Ca(OH)2, dość mocnej zasady. Stosowana do wykrywania dwutlenku węgla. Wydmuchując powietrze do zlewki wypełnionej wodą wapienną, pojawia się białe jak mleko zmętnienie. Wytrąca się bowiem ciemnokrystaliczny biały osad węglanu wapniowego.
Rys. 4 Prosta aparatura, umożliwiająca przeprowadzenie próby na obecność dwutlenku węgla; rezultat pozytywnego wyniku próby

Ad. 5
Woda ciężka to tlenek jednego z izotopów pierwiastka wodoru – deuteru. Jej małe ilości są w zwykłej wodzie. Ciężka woda stosowana jest jako moderator w reaktorach jądrowych do spowalniania szybkich neutronów. Z tego powodu, w czasie ostatniej wojny odegrała ważną rolę strategiczną. Znalazło to swoje odbicie w filmie pt. „Bitwa o ciężką wodę”. Ta „bitwa” był to całokształt akcji podejmowanych w celu opóźnienia prowadzonych prze hitlerowskie Niemcy prac nad bronią atomową. Dowództwo alianckie z tego powodu zdecydowało się zniszczyć zakład chemiczny Norsk Hydro, który ówcześnie produkował ciężką wodę na skale przemysłową. Oprócz filmu, na podstawie tej historii w 2015 roku powstał norweski serial telewizyjny o tym samym tytule.
Rys. 5 Hydroelektrownia Norsk Hydro- przykłady wyposażenia, które zostało zniszczone podczas II wojny światowej; reaktor ciężkowodny w Iranie.

Ad. 6
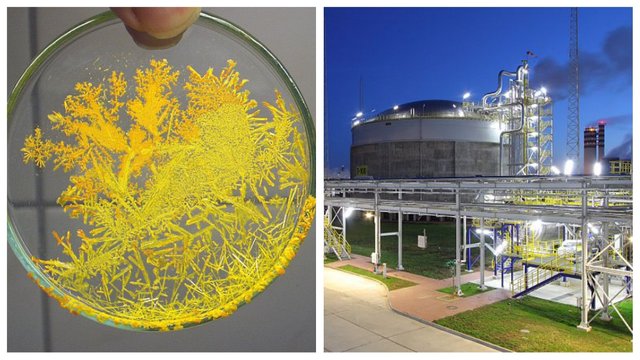
Woda amoniakalna jest to wodny roztwór amoniaku o stężeniu od 10% do 25%. Wydziela ostry, nieprzyjemny zapach amoniaku. Wykorzystywana w wielu gałęziach przemysłu.
Rys. 6 Kryształy dichromianu amonu (NH4)2Cr2O7; zakłady azotowe „Puławy”-największy w Polsce zakład w branży wielkiej syntezy chemicznej, produkcja samej tylko saletry amonowej wynosi ok. 1 100 00 ton na rok.
Inne zagadki: Metale; Metale II
Źródła grafik:
Rys. 1 by: Andres Punning; by: Thejohnnler
Rys. 2 by: Ellen Sharples ;by: Spiff; by:Mateus S. Figueiredo
Rys. 3 by:DavidAndrew54; by:Olli Niemitalo
Rys. 4 by:Gregory, R. A Simmons, A. T; by:tjmwatson
Rys. 5 by:martin_vmorris; by:Nanking2012
Rys. 6 by:W. Oelen; by:Kowal kowal
Zaczerpnięte z: „500 zagadek chemicznych” Marta Jurowska – Wernerowa , Warszawa 1980
Congratulations @conven! You have completed the following achievement on Steemit and have been rewarded with new badge(s) :
Click on the badge to view your Board of Honor.
If you no longer want to receive notifications, reply to this comment with the word
STOPTo support your work, I also upvoted your post!
Do not miss the last post from @steemitboard:
SteemitBoard World Cup Contest - The results, the winners and the prizes