Nrf2: Das zelluläre Wächterprotein gegen oxidativen Stress. [ger]
Wie sich unsere Zellen gegen oxidative Schäden schützen und wie dieses System durch Lebensmittel beeinflusst werden kann.

Wahnsinn, ich kann für einen Wissenschaftspost ein mystisches Bild verwenden. Wächter und so... CC0, von pixabay
Intro
Eigentlich wollte ich diese Woche eine Auftragsarbeit für den guten @felixxx schreiben, der mich schon auf die Östrogen-Schiene gestoßen hat… wofür ich nach wie vor nicht weiß, ob ich ihm danken oder ihn verfluchen soll. ;-P
Wie dem auch sei, ich kann das von ihm angeregte Thema nicht erledigen, ohne vorab ein paar Basics zu (er)klären. Sulforaphan kommt dann in Kürze, versprochen.
Worum geht es also hier und heute? Um oxidativen Stress. Yay. Ein Modewort in jedem Hipster-Ernährungs-Lifestyle-Bullshit-Magazin, dass was auf sich halten will.
Und darum, wie der Körper auf diesen antwortet. Also wird's zur Abwechslung wieder ein bisschen molekularbiologisch. Anschnallen bitte, los geht’s.
Reaktive Sauerstoffspezies
Als ROS (engl. reactive oxygen species) bezeichnet man eine Gruppe von kleinen Sauerstoff-haltigen Molekülen, die bei verschiedenen biochemischen Reaktionen, insbesondere bei den Reaktionen des Stoffwechsels, als Nebenprodukte anfallen. Es handelt sich dabei um verschiedene Radikale wie z.B Superoxid (O2-), das Hydroxylradikal, Peroxid- und Alkoxylradikale usw. aber auch nicht-radikalische Oxide wie z.B. Wasserstoffperoxid oder Singulett-Sauerstoff.
Wie den Schlauis unter meinen Lesern sicher aufgefallen ist, deutet das R in ROS schon darauf hin, warum diese ein potentielles Problem darstellen... Sie sind reaktiv. Und zwar ziemlich. Sie oxidieren und schädigen alle Makromoleküle, die ihnen so in die Quere kommen. Und nachdem sie vor allem beim Metabolismus gebildet werden, der in den Mitochondrien und damit in den Zellen stattfindet, haben sie gleich nach Entstehung mehr oder weniger die freie Wahl.
Zelluläre Fette, Proteine oder – besonders „lustig“ – unsere Gene… nichts ist vor ihnen sicher.
Das kann sich eine selbstbewusste Zelle natürlich nicht bieten lassen, und produziert dagegen sogenannte Phase II Enzyme (z.B. Glutathion)*, deren Hauptaufgabe es ist, ROS und andere Schadstoffe einzufangen und zu binden, bevor diese Schaden anrichten können.
Prinzipiell sind unsere Zellen also gut gegen ROS gerüstet, und für manche Prozesse sind diese auch sehr wichtig, wie z.B. für das Muskelwachstum.
*Wer wissen will, welche Bedeutung Phase II Enzyme im Fremdstoffmetabolismus haben, möge in diesem alten englischen post von mir nachlesen.
Oxidativer Stress
Ein Problem kriegt die Zelle nur dann, wenn durch externe Einflüsse plötzlich die Menge der vorhandenen Phase II Enzyme nicht mehr ausreicht, um die intrazellulären ROS in Schach zu halten. Das kann auf zwei Wegen passieren:
- Es sind plötzlich viel mehr ROS vorhanden, weil z.B. Stoffe aufgenommen wurden, die ROS produzieren wie Sau. Hände hoch, ihr Raucher!
- Die Phase II Enzyme werden benötigt, um andere Fremdstoffe zu neutralisieren.
Beides führt dazu, dass die ROS nun plötzlich doch in der Lage sind, die Zelle zu schädigen, was der Zustand ist, den man als „oxidativen Stress“ bezeichnet.
Regelmäßiger oder gar chronischer oxidativer Stress wird mit einer Reihe von Zivilisationskrankheiten assoziiert, wie z.B. Herz-Kreislauferkrankungen, neurodegenerative Erkrankungen (z.B. Alzheimer), und natürlich Krebs (da oxidative DNA-Schäden Mutationen auslösen und dadurch Zellen zum „Entarten“ bringen können).
Was der Grund ist, warum Antioxidantien zur Zeit so in Mode sind. Dass diese wahrscheinlich nicht helfen… geschenkt. Darum soll es heute nicht gehen.
In diesem Post geht es darum, was die Zelle selbst macht, wenn sie merkt, dass sie sich im oxidativen Stress befindet.
Das zelluläre Schutzsystem und Nrf-2
Zellen nehmen die oxidative Gefahr nämlich keineswegs einfach hin. Der erste Schritt zur Verteidigung ist immer, zu erkennen, dass überhaupt Gefahr droht. Dazu produziert die Zelle ein Protein mit dem etwas sperrigen Namen „nuclear factor (erythroid-derived 2)-like 2“, den man aber Gott sei Dank einfach mit Nrf-2 abkürzen darf.
Ja ich weiß, Biologen… Können’s das Teil nicht einfach Spiderman nennen und gut ist?
Nrf-2 ist im Zellplasma an ein anderes Protein namens KEAP1 (den Langnamen erspar‘ ich euch) gebunden, das dafür sorgt, dass das Nrf-2 ständig wieder abgebaut wird.
Wenn aber die ROS überhand nehmen, attackieren diese den KEAP1/Nrf-2 Komplex, was Nrf-2 freisetzt. Dieses wird dann nicht mehr abgebaut, sondern akkumuliert sich in der Zelle und gelangt schließlich sogar in den Zellkern. Dort angekommen, bindet es an die DNA, und zwar an eine eigens dafür konzipierte Stelle, das sogenannte „anti-oxidative responsive element“ (ARE).
Das ARE liegt in der sogenannten „Promoterregion“ von Genen, d.h. in den DNA-Stücken, die direkt vor dem eigentlichen Gen liegen, und so zwar nicht für Proteine codieren, aber an der Regulierung von Genen mitarbeiten. Die Promoterregion entscheidet letztlich darüber, ob ein Gen „transkribiert“ (=in RNA übersetzt) und in weiterer Folge das zugehörige Protein „exprimiert“ (=produziert) wird. Dafür werden sogenannte Transkriptionsfaktoren verwendet, also Stoffe, die an die Promoterregion binden können, und dann das Gen ein- oder ausschalten bzw. seine Transkription verstärken oder verringern.
Nrf-2 ist der zugehörige Transkriptionsfaktor für ARE, und zwar ein Aktivator. Bindet Nrf-2 an ARE, schaltet es also die nachgelagerten Gene an.
Welche Gene sind das?
Das ARE findet man vor vielen Genen, die für die weiter oben erwähnten Phase II Enzyme codieren.
Oder auf Deutsch: Nrf-2 erkennt, dass die Zelle zu wenige Phase II Enzyme hat, um mit dem aktuellen ROS Spiegel mitzuhalten, und sorgt dann gleich selbst dafür, dass die Zelle diese vermehrt produziert.
Und so verteidigt sich die Zelle selbst gegen oxidativen Stress, ganz ohne Antioxidantien.
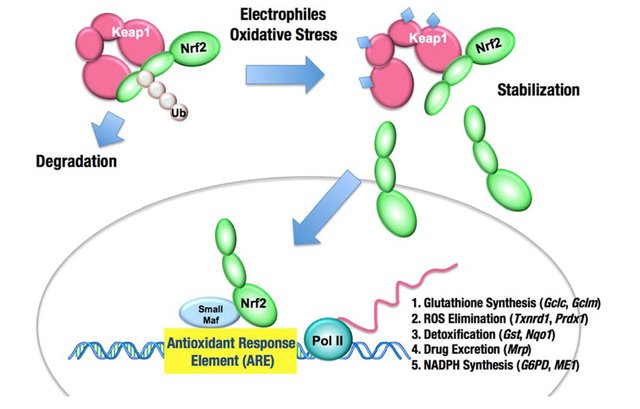
Eine schematische Darstellung der zellulären Verteidigungsstrategie gegen ROS, mit Nrf-2 in der Hauptrolle. Quelle: Mitsuishi, Motohashi and Yamamoto, Frontiers in Oncology, CC-BY 3.0
Was heißt das jetzt für uns?
Unser Körper kommt in der Regel recht gut mit oxidativem Stress klar. Wenn man bedenkt, dass wir zusätzlich zum körpereigenen Wächtersystem auch noch wirksame Antioxidantien wie z.B. Vitamin C und E aufnehmen, ist der logische Schluss eigentlich, dass eine zusätzliche Aufnahme von direkt anti-oxidativ wirksamen Substanzen nicht wirklich notwendig ist (direkt im Sinne von Radikalfängern).
Und tatsächlich lässt sich ein gesundheitlicher Vorteil von Heidelbeere, Rotwein & Co in Humanstudien kaum feststellen. Dieser ist - wenn überhaupt vorhanden - marginal.
Aber es gibt Stoffe, die spielen in einer anderen Liga. Wenn eine Substanz nämlich in der Lage ist, den Nrf-2 Weg zu stimulieren, kann ihre regelmäßige Einnahme dazu führen, dass Phase II Enzyme dauerhaft überexprimiert werden, was zur Folge hat, dass die Zellen des Körpers generell seltener unter oxidativem Stress zu leiden haben.
Dieses Konzept spielt bei der chemopräventiven, also krebsvorbeugenden, Wirkung von Lebensmitteln eine große Rolle.
Das Problem dabei ist allerdings, dass ein Stoff das Nrf-2 System nur aktivieren kann, wenn er selbst oxidativen Stress verursacht. Diese Situation mag zuerst paradox klingen, hat aber sogar einen eigenen Fachbegriff: die Hormesis.
"Hormesis" ist eine auf Paracelsus zurück gehende Hypothese, nach der bestimmte Stoffe in geringen Dosen gesundheitsfördernd, in höheren Dosen aber toxisch wirken.
Eine geringe Menge eines ROS-Produzenten führt wie erwähnt zur Induktion des Nrf-2 Sytems und dadurch zur gesteigerten Abwehrkraft des Körpers gegen eine oxidative Schädigung, ohne dass bedeutende Zellschäden auftreten. Nimmt man vom selben Stoff eine größere Menge auf, induziert man zwar auch Nrf-2, schädigt die Zellen aber so, dass der Schaden den Nutzen übersteigt.
Oder anders ausgedrückt: Isst man ab und zu Broccholisprossen, kann das durchaus gesund sein. Sich Sulforophan-Ergänzungsmittel in Überdosierung einzuwerfen, ist keine gute Idee. Aber mehr dazu dann in Kürze.
Quellen:
Ich habe mich während meiner wissenschaftlichen Tätigkeit schon öfter mit Nrf-2 beschäftigen müssen (dürfen), und habe das Meiste daher ohne groß nachzulesen runtergeschrieben. Kleinigkeiten nachgeschaut bzw. auf Richtigkeit überprüft habe ich bei:
Mitsuishi et al., 2012: "The Keap1–Nrf2 system in cancers: stress response and anabolic metabolism", Front Oncol.
Sestili und Fimognari, 2015: "Cytotoxic and Antitumor Activity of Sulforaphane: The Role of Reactive Oxygen Species", Biomed Res Int
Ma, 2013: "Role of Nrf2 in Oxidative Stress and toxicity", Ann Rev Pharm Tox.
...und natürlich Wikipedia...
Disclaimer:
In meinem Blog schreibe ich meine ehrliche Meinung als toxikologischer Forscher, nicht mehr und nicht weniger. Ich bin ein Mensch, manchmal unterlaufen mir Fehler. Diskutiert mit mir, seid anderer Meinung – wenn ihr die besseren Argumente bringt, überleg‘ ich gern ein zweites Mal.
Ich komme mir sehr ertappt vor. Ich habe gerade an alle Momente zurückgedacht, in denen ich andere von einem Lebensmittel zu überzeugen versucht habe, weil sie "antioxidant" sind. :D
Gibt es noch weitere Stoffe, abgesehen vom Sulforaphan, die diese Phase II Enzyme exprimieren?
Kleine Korrektur: Stoffe exprimieren keine Enzyme, sie bringen die Zellen dazu, Enzyme zu exprimieren.
Aber ja, es gibt jede Menge Nrf2 Aktivatoren. Oft wird in Berichten nicht zwischen direkten Antioxidantien und indirekt anti-oxidativen Stoffen, die halt über Nrf2 wirken, unterschieden.
Gut möglich also, dass du mit deinen Ernährungsempfehlungen trotzdem teilweise nicht mal so falsch lagst. ;-P
Hi @sco!
Your post was upvoted by utopian.io in cooperation with steemstem - supporting knowledge, innovation and technological advancement on the Steem Blockchain.
Contribute to Open Source with utopian.io
Learn how to contribute on our website and join the new open source economy.
Want to chat? Join the Utopian Community on Discord https://discord.gg/h52nFrV
Super Artikel.
Hab gerade einen Mexidol/Emoxipin Cycle durch, weil es eben mit Nahrungsmitteln kaum therapeutischen Effekt gibt. Was die Hipsters aber vergessen, es gibt auch das Konzept des Anti-Oxidativen Stresses. ROS leitet Regenerationsprozesse ein was dazu führt, dass man sich mit Vitamin E rund ums Training den Effekt zerschießen kann. Es war ja auch lange Zeit kontrovers Diskutiert warum man bei starken Rauchern mit (vermutlich vorhandenem Krebs) bei hoher Vitamin E Gabe eine höhere Mortalität auftritt :D
voll. Kurzfristiger oxidativer Stress kann notwendig sein. Der chronische ist ein Problem.
Hello, as a member of @steemdunk you have received a free courtesy boost! Steemdunk is an automated curation platform that is easy to use and built for the community. Join us at https://steemdunk.xyz
Upvote this comment to support the bot and increase your future rewards!
Ein wirklich grossartiger Artikel!
Kannst du denn ausser hochdosierten Brokkoli-Kram noch andere Dinge nennen, die den Prozess auslösen? Wär mega spannend, finde ich.
Danke, und danke auch fürs lesen&kommentieren!
Ja, da gibt's schon einiges: Das Sulforophan in Kohlgemüse (v.a. in Broccholisprossen) hab ich schon erwähnt, Curcumin in Curcuma, oder natürlich catecholische Verbindungen wie z.B. Quercetin, das in wirklich vielen Lebensmitteln vorkommt (Zwiebel, Äpfel, Kapern, Schnittlauch,...).
Super Artikel. Bestätigt wieder einmal, dass Prozesse im Körper immer differenziert betrachtet werden müssen.
Danke.