INDICADORES ÁCIDO-BASE
Saludos estimada comunidad de Steemit y en especial a Steem-espanol.
Muchos compuestos orgánicos tanto naturales como sintéticos tienen un color que cambia según el pH. Esto no solo agrega belleza y variedad a nuestro entorno, sino que es una propiedad química muy útil.
Para los que hacemos ciencia y hemos trabajando dentro de un laboratorio es muy probable que alguna vez lleváramos a cabo una titulación ácido-base y, antes de iniciarla, tuvimos que agregar un indicador. Antes de entrar en materia es de suma importancia definir que es la escala de pH y que es un indicador ácido base.
ESCALA DE pH
Se trata de una unidad de medida de alcalinidad o acidez de una solución, más específicamente el pH mide la cantidad de iones de hidrógeno que contiene una solución determinada.
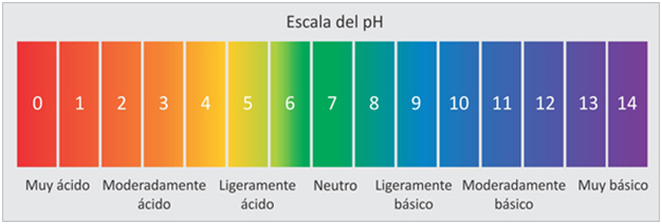
El pH de una disolución se define como el negativo del logaritmo en base 10 (log) de la concentración de iones de hidronio.
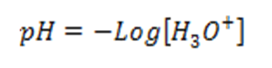
Ec. 1
INDICADORES ÁCIDO-BASE
El indicador ácido-base suele ser un compuesto orgánico que es en sí un ácido débil o una base débil, estos compuestos tienen una características que los hace sumamente útil y es que son compuestos cuyo color es sensible al pH, es decir, que tienen cierta coloración al estar en una solución ácida y otra diferente al encontrarse en una solución básica. Entre los indicadores ácido-base más utilizados podemos encontrar fenolftaleína, anaranjado de metilo, azul de metileno, entre otros.
Uno de los indicadores más conocidos es la fenolftaleína, que es incoloro en medio ácido y rosa en medio alcalino (se utiliza mucho en series como CSI). Muchas sustancias comunes como el té, vino tinto, extracto de flores y el repollo colorado presentan distintos colores según el pH del medio. Para poder utilizarlos como indicadores, es necesario investigar con ácidos o bases conocidas, que color toman.
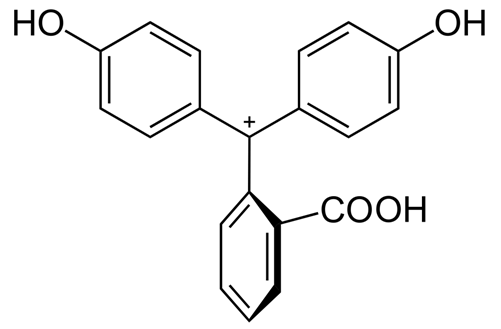
Figura 2. Estructura química del indicador fenolftaleína
¿CÓMO FUNCIONAN LOS INDICADORES ÁCIDO-BASE?
Al adicionar un indicador a una muestra, generalmente una disolución, sobre la que se deseamos realizar el análisis, este empieza a producir un cambio químico en el que es apreciable, generalmente, un cambio de color en el indicador. Este cambio ocurre porque estas sustancias sin ionizar tienen un color distinto al que tienen cuando están ionizadas.
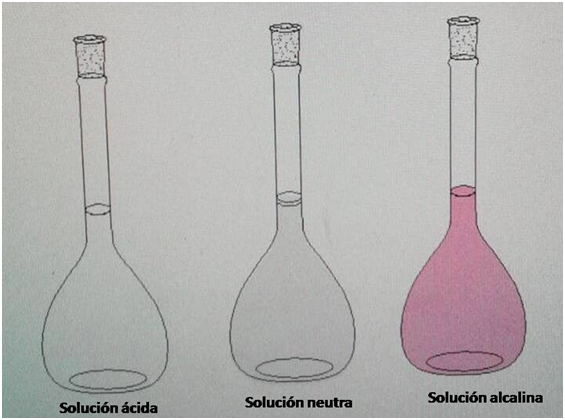
Figura 3. Cambio de color de una solución según su pH utilizando fenolftaleína como indicador-Fuente: Elaboración propia.
La mayoría de los indicadores son de hecho ácidos débiles por si mismos, por lo que son capaces de reaccionar tanto con ácidos como bases. Cada reacción produce un color diferente. Esa es la razón por la cual los indicadores son capaces de cambiar el color de una solución.
Desde un punto de vista molecular los indicadores son colorantes con una estructura relativamente compleja cuyo color cambia según estén en presencia de un medio ácido o un medio básico. La variación de color se denomina viraje. En la figura 4 podemos apreciar como cambia el color del indicador fenolftaleína cuando varia el pH de una disolución.
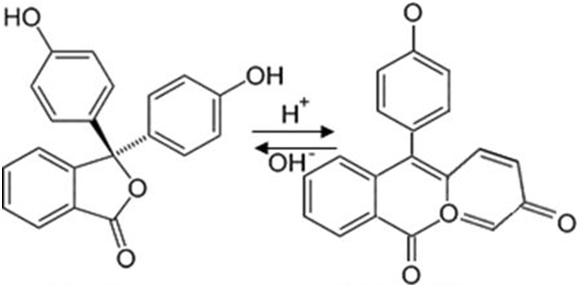
Figura 4. Cambio estructural del indicador fenolftaleína segúnel pH
RANGO DE VIRAJE
El cambio de color del indicador se denomina viraje, y el intervalo de pH en el que se produce el cambio de color, es lo que se denomina intervalo de viraje. Cada uno de los indicadores posee un intervalo de viraje que lo caracteriza, es decir, un entorno en mayor o menor medida, reducido de unidades de pH. Dentro de dicho intervalo es donde se produce el cambio de color, o viraje. Un indicador tiene mayor utilidad, cuanto más pequeño es su intervalo de viraje, produciéndose así de forma más clara y sencilla el cambio de color.
En la tabla siguiente se muestran algunas indicadores ácidos-base, junto a los datos de sus intervalos de viraje y el color que tienen cuando el pH es menor o superior a dicho intervalo.

Tabla 1. Intervalo de viraje de algunos de los indicadores ácido-base más utilizados. Elaboración propia.
¿POR QUÉ SON TAN IMPORTANTES LOS INDICADORES ÁCIDO-BASE?
Prácticamente en todos los procesos que se llevan a cabo en la industria el control de los niveles de pH de los productos, soluciones y materiales que se fabrican es un factor de gran importancia, es por esto que son las sustancias a las cuales llamamos indicadores ácido-base son tan relevantes. La medición del potencial de hidrógeno es considerada como un indicador de calidad de los productos y por ello las diferentes autoridades reguladoras de la industria han impuesto normativas para la producción y las características que debe cumplir un producto para ser lanzado al mercado.
Una de las características que deben ser controladas de manera precisa en la industria es el nivel de pH de los productos, sobre todo en la industria cosmética, farmacéutica y alimentaria. Por lo anterior, el uso de indicadores de pH en la industria de los alimentos es de suma importancia, pues las normativas respecto a este parámetro son estrictas y sus objetivos principales son evitar la contaminación del medio ambiente y garantizar que el producto final que se ofrece al consumidor esté libre de microorganismos que puedan provocar algún daño.
Pero hay otras razones por las que verificar el nivel de acidez o alcalinidad de los productos y materias que se utilizan para la producción de los alimentos es importante. Por ejemplo, estos valores sirven para conocer e incrementar el tiempo de conservación del producto o para conocer la forma de acción de los bactericidas que se aplican para eliminar microorganismos del producto.
Un producto en el que paso tras paso de su proceso de producción se debe medir el potencial de hidrógeno es el azúcar. La importancia de medir este coeficiente es para evitar y eliminar cualquier tipo de contaminación e impurezas en el producto. El nivel máximo permitido es 7; un nivel mayor implicaría que el jugo de caña se convertiría en miel.
Como estos existen muchos otros ejemplos, pues prácticamente todos los productos pasan por un proceso de medición de acidez o basicidad para garantizar su calidad, sabor e higiene. En algunos casos el nivel debe ser muy preciso, pero en otros basta con que el producto esté por encima o debajo de cierto nivel.
Sea cual sea el caso, el uso de indicadores de pH es fundamental e imprescindible en la industria alimentaria para garantizar la calidad de los diferentes productos que se fabrican. Dependiendo de la industria y del producto se requieren diferentes métodos para medir la acidez o basicidad de las sustancias y materiales utilizados. Por ello las empresas requieren contar con un proveedor que ofrezca diferentes opciones para conocer los niveles de pH, según sus necesidades.
REFERENCIAS
- John Kotz, Treichel Paul, Quimica y reactividad química, quinta edición, 2003.
- Intervalo de viraje
- Importancia de los indicadores ácido-base
Estimada @mayterevilla muy buen post. Ciertamente uno de los químicos mas empleados para la determinación de concentraciones desconocidas. Muy útil tu información. saludos.
Gracias por leerme siempre amiga, saludos!
¡Felicitaciones tu publicación ha sido seleccionada para recibir el Upvote y Resteem del Proyecto de Curación @Codebyte!
Si deseas apoyarnos y saber mas sobre este proyecto puedes seguirlo y estar atento a sus publicaciones. Ingresando aquí podrás ver el reporte en donde tu publicación ha sido destacada.
La Química es una ciencia muy hermosa y post como el tuyo nos hacen recordar las bases sobre las que se fundamenta gran parte de esa belleza. Los indicadores son parte fundamental en la caracterización de las sustancias.
Graaaacias!
Muy buen post, estimada @mayterevilla muy util tu información a la hora de entender a estos compuestos tan utilizados dentro del laboratorio. Saludos.
Gracias mi estimada, saludos para ti.
Resteemed your article. This article was resteemed because you are part of the New Steemians project. You can learn more about it here: https://steemit.com/introduceyourself/@gaman/new-steemians-project-launch