Análisis termogravimétrico (TGA). Aplicación al estudio del ácido tungstofosfórico.
Saludos estimada comunidad científica de steemit y de #stem-espanol.
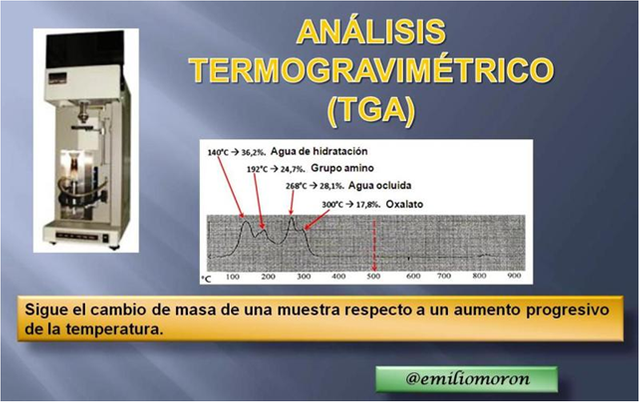
Figura 1. Ilustración de un analizador y el reporte generado. Fuente: composición de imágenes propia.
En esta publicación les comentaré sobre la técnica, y en mi caso, como la usé como punto de partida para la caracterización del ácido tungstofosfórico, compuesto que utilicé como precursor de un catalizador de tungsteno, a fin de establecer el mejor rango de temperatura en el cual se haría el tratamiento de síntesis y la fase en la que se esperaba trabajar.
Algunos fundamentos
Los efectos que puede generar la variación de la temperatura sobre un material son diversos, y además se pueden producir cambios en muchas propiedades. Pero en el análisis termogravimétrico (TGA) el seguimiento a los cambios de masa constituyen la base del estudio. En otros tipos de análisis térmico, el seguimiento de los cambios de energía son el fundamento del análisis termodiferencial (TDA) y de la calorimetría diferencial de barrido (DSC); de este modo, mientras el TGA nos expresa la pérdida de masa de masa una muestra y cuanto, el TDA nos dice si esta reacción o proceso de cambio físico es endotérmico o exotérmico.
Métodos de análisis termogravimétricos
El TGA consiste en registrar de forma continua la variación de masa que experimenta determinado material, colocado en una atmósfera contralada, conforme la temperatura aumenta progresivamente a una tasa constante, este caso se conoce como análisis dinámico, otra opción es realizar el análisis manteniendo constante la temperatura todo el tiempo que se establezca para el experimento, a este se le conoce como análisis isotérmico. A la representación gráfica de la variación de la masa en función de la temperatura, o el tiempo, se le denomina termograma.
En la siguiente figura se describe la representación típica de un termograma.
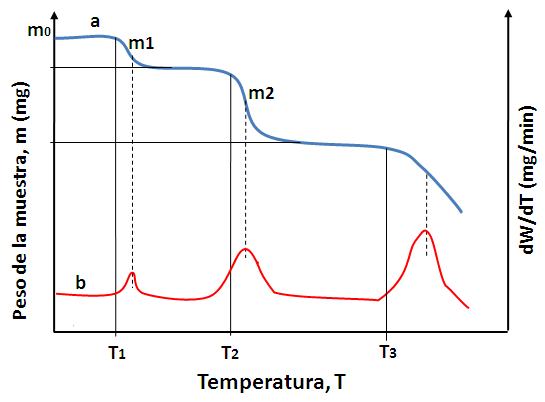
Figura 2. Termograma a) convencional (curva azul y eje izquierdo), b) diferencial (curva roja y eje derecho).
Instrumentación
Los modernos instrumentos empleados para este tipo de análisis tienen como principales partes: a) una balanza analítica, que es capaz de proporcionar información cuantitativa de la masa de la muestra, comúnmente en un intervalo entre 5 y 20 mg, b) un horno donde se encuentra situado el soporte de la muestra, en la mayoría de los hornos la temperatura se puede incrementar desde la temperatura ambiente hasta 1000 ºC, e igualmente se puede variar la velocidad de calentamiento, para evitar la transferencia de calor a la balanza el horno se encuentra aislado de la misma, c) un sistema de gas de purga, que generalmente puede ser nitrógeno o argón, que se utiliza para desplazar el aire de la cámara de la muestra y evitar la oxidación de la misma. Y d), un microprocesador para el control del instrumento y el procesamiento de los datos.
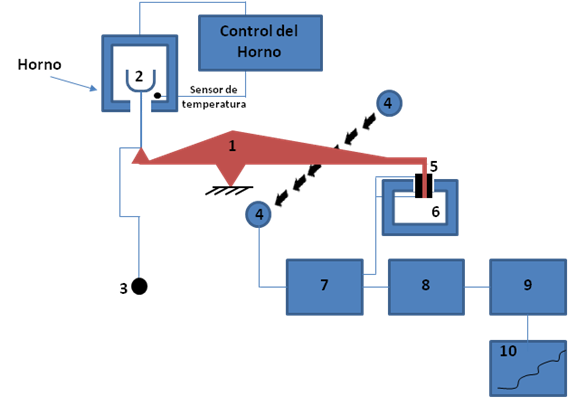
Figura 3. Esquema del diseño de una termobalanza. 1) Brazo, 2) soporte de la muestra, 3) contador de peso, 4) lámpara y fotodiodos, 5) bobina, 6) imán, 7) control del amplificador, 8) calculador de Tara, 9) amplificador, 10) registro. Fuente: elaboración propia, adaptado de Skoog (2002).
Como se puede apreciar en la figura 3, un cambio de masa en la muestra produce una desviación del brazo, el cual se interpone al paso de luz entre la lámpara y uno de los fotodiodos; la disminución de la corriente fotodiódica se amplifica y se alimenta a una bobina que se ubica entre los polos de un imán, el campo magnético generado por la bobina restablece la posición inicial del brazo. La corriente amplificada del fotodiodo se recoge y se transforma en información relativa a la pérdida de masa de la muestra, los cuales son representados inmediatamente en un registrador o pueden ser almacenados para un procesamiento posterior dependiendo del equipo.
Preparación de la muestra
En general la disposición de la muestra para realizar el ensayo no requiere de una difícil preparación, solo debemos acomodar una pequeña cantidad de la muestra en el contenedor o portamuestra, pero es muy importante asegurarnos que éste se encuentre totalmente limpio antes de colocarla, se considera que una masa apropiada de muestra para su análisis es de aproximadamente 10 o 20 mg, nunca sobrepasando los 50 mg.
Una vez acomodada la muestra en el contenedor, este se suspende en el interior del horno, colgándolo de un soporte en forma de gancho.
Figura 4. Ilustración de la manipulación de la muestra para colocarla en el interior del horno. Fuente: elaboración propia.
Descripción del ensayo para el análisis del ácido tungstofosfórico.
Para determinar la estabilidad del ácido tungstofosfórico (H3PW12O40), el cual fue empleado como precursor para la síntesis de un catalizador a base de tungsteno, se efectuó el análisis termogravimetrico bajo atmósfera reductora (H2); mediante este análisis se determinó la vía y temperatura de descomposición del sólido.
Antes de realizar el análisis debemos tarar el brazo de la balanza, verificar el flujo de gas y definir la rampa de temperatura para el calentamiento. Para mi análisis se colocaron 10 mg de la muestra y se estableció un intervalo de temperatura de 25 a 900 ºC a una razón de 10 ºC/min, mediante un analizador tipo Dupont 945. Con la muestra en posición se cierra la cámara térmica y se inicia el análisis en las condiciones establecidas, a medida que progresa el calentamiento el equipo registra los cambios de masa en el sólido. En la siguiente figura se muestra el termograma obtenido para el H3PW12O40.
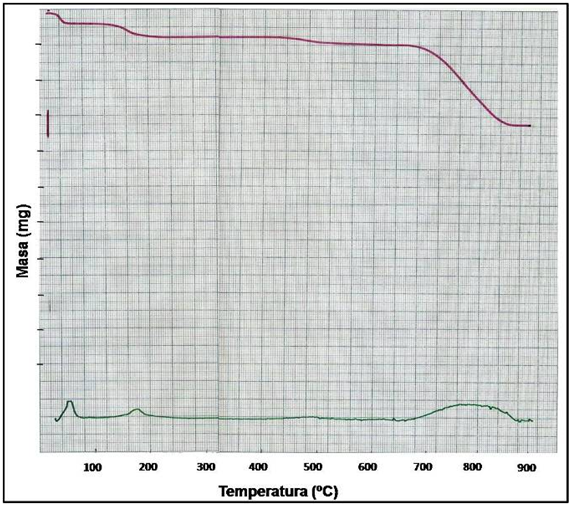
Figura 5. Termograma correspondiente a la descomposición del H3PW12O40 en atmosfera de hidrogeno. Fuente: propia.
En la gráfica se observa una pérdida progresiva de masa (curva superior de color rojo), las primeras inflexiones en la curva, reflejadas a 60 ºC y 180 ºC se deben a la evaporación del agua absorbida por el sólido. Por encima de 200 ºC se ha evaporado toda el agua y se obtiene la estructura primaria del ácido, la cual se mantiene hasta una temperatura cercana a los 450 ºC donde se observa otra inflexión en la curva, esta es debida a la perdida de agua correspondiente a la perdida de protones del ácido originando la descomposición de este en P2O5 y WO3; estos compuestos persisten hasta una temperatura cercana a los 650 ºC, donde se puede observar una fuerte variación en la masa, indicando la descomposición de estos compuestos. Según la pérdida de masa se puede describir la vía de descomposición del ácido tungstofosfórico en atmósfera reductora de la siguiente forma:
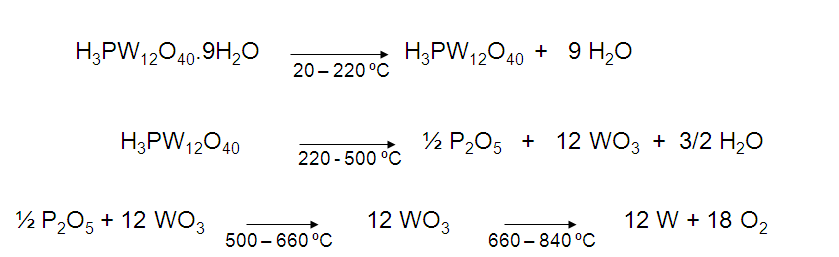
Esta secuencia fue comprobada comparando la disminución porcentual de masa registrada en el TGA con la pérdida de masa teórica según cada paso con la siguiente expresión:
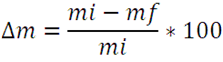
Donde ∆m es el cambio porcentual en masa, mi la masa inicial y mf la masa final reportada en cada cambio. Así, en la primera inflexión observada a 60 ºC, se registró una pérdida de masa de 0,25 mg, lo que correspondería con una pérdida del 2,5% de la masa inicial. Como se muestra en la siguiente tabla.
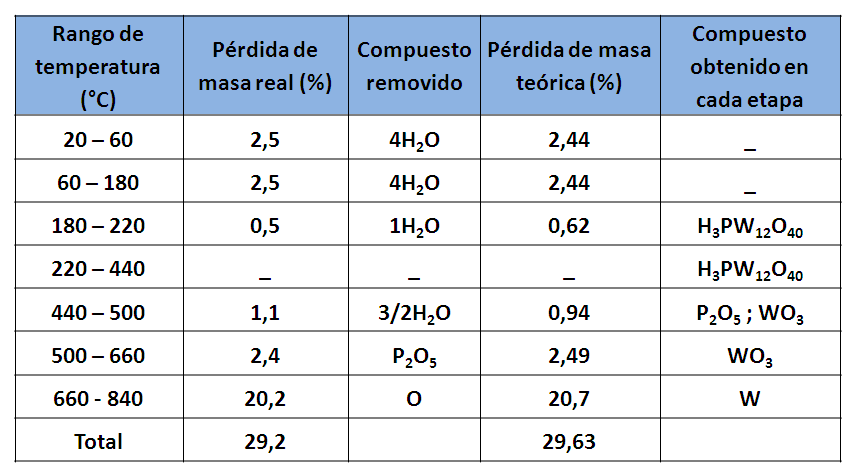
La curva inferior de color verde en el termograma, corresponde a la derivada de la masa en función de la temperatura,
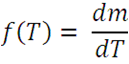
En este caso es representada la pérdida de masa con la variación de la temperatura, pudiendo identificar la temperatura a la cual ocurren los cambios importantes de masa, es decir donde se registra la descomposición.
Discusión
Los termogramas aportan información importante para establecer el mecanismo de descomposición de un sólido. Y a los fines de la síntesis del catalizador buscado, se deseaba trabajar con la fase de óxido del compuesto, por lo que mediante el análisis realizado se logró establecer que para el tratamiento de síntesis se debía realizar la operación en el rango de temperatura de 500 a 600 ºC.
Aplicaciones cuantitativas
A diferencia de la gravimetría de precipitación, que tiene más fines prácticos en los laboratorios, la termogravimetría desempeña un papel importante en el análisis químico, por ejemplo, se emplea en la determinación de cenizas en muestras de papel o en la determinación de la estabilidad de polímeros y el contenido de aditivos en los plásticos, detección del contenido de agua para el control de calidad en compuestos farmacéuticos y alimenticios, así como determinación de componentes volátiles. Otro ejemplo es su utilización para determinar el contenido de sólidos disueltos en el agua y en aguas residuales, para ello la muestra se somete a calentamiento hasta alcanzar un peso constante, la muestra secada a la temperatura más baja contiene agua ocluida y a temperaturas más altas ocurren pérdidas de carbonatos, cloro, nitrógeno y material orgánico.
En fin estimados amigos, el TGA es una versátil técnica que puede ser empleada para investigar cualquier proceso físico o químico que se manifieste por un cambio de peso del material al ser sometido a calentamiento. Y con un poco de pericia estequométrica se pueden realizar estimaciones cuantitativas del mismo.

Referencias
Harvey, D. (2002). Qímica Análtica Moderna. McGraw-Hill.
Morón, E. (2010). SINTESIS Y EVALUACION DE CATALIZADORES DE NITRUROS DE TUNGSTENO Y MOLIBDENO SOPORTADOS EN ALUMINA PARA LA HDS DE TIOFENO. UNEFM.
Rodriguez, E. (2012). Caracterización de polímeros aplicando el método termogravimétrico. Métodos y materiales, vol.2, 24-32.
Skoog, D., West, D., Holler, F. Crouch, S.; (2003). Química Análitica. Séptima edición, McGraw-Hill.
que buen trabajo se ve te gustan los números
Gracias amigo. A veces te puedes divertir con la estequimetría jeje.
Como siempre muy buen aporte el que muestras mi estimado, excelente artículo @emiliomoron. Saludos
Gracias mi estimada @maurelvys, me complace que te haya gustado. Mis saludos y gracias por comentar!