Equilibrio Químico: Del dinamismo a lo constante.


Conceptos Importantes
El equilibrio químico es una de las áreas más estudiadas de la química. Una gran cantidad de compuestos presentes en la naturaleza coexisten con otros compuestos en un equilibrio químico, en el cual el producto de las concentraciones es constante en todo momento. Estos conceptos también representan una gran importancia para la industria moderna, ya que permite calcular el valor teórico de las concentraciones de los reactantes producido en un reactor o la cantidad de soluto disuelto en algún contenedor. Estas propiedades fisicoquímicas han sido mejoradas con el pasar los años, a tal punto que se han logrado calcular constantes de equilibrio bastante exactas a diferentes temperaturas, e incluso encontrar alguna función matemática dependiente de la temperatura (como variable) para obtener valores a distintas temperaturas. Dada una reacción química general, su constante de equilibrio para las concentraciones será:
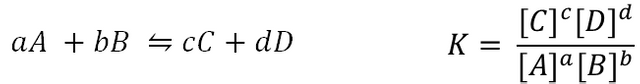
Equilibrio Químico:
En un proceso químico, el equilibrio químico es el estado en el que las actividades químicas o las concentraciones de los reactivos y los productos no tienen ningún cambio neto en el tiempo.
Si hay dos estados de agregación de la materia, entonces es Heterogéneo. Los estados Liquido (l), y Solido (s) no afectan la constante especifica de velocidad K (no intervienen en el equilibrio).
Muchas personas al escuchar la palabra “Equilibrio”, la asocian con el equilibrio físico, fenómeno bastante cotidiano que nos acompaña incluso desde que éramos niños, en caricaturas, al ver algún malabarista en el circo, o simplemente cuando observamos a los niños jugar en un columpio. Por lo tanto, es bastante familiar observar y entender la figura a continuación:

Es evidente, que cada uno de los cuadrados pesa exactamente lo mismo, y por lo tanto la plataforma no se inclina hacia ninguno de los lados, se dice que el sistema esta en equilibrio. Aun así, extraer esta analogía y aplicarlo en el equilibrio químico, es una de las grandes fallas de los estudiantes (la cual le genera gran confusión a primera vista). En este caso el equilibrio químico que se presenta, no tiene porque ser equitativo, si tuvieras que aplicar la misma analogía, un equilibrio químico puede ser representado de la siguiente manera:
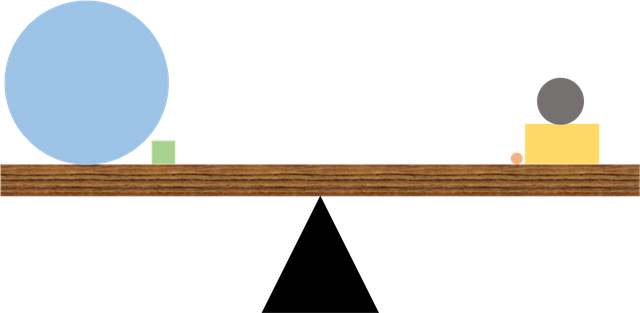
Es extraño a simple vista, pero los equilibrios químicos no necesariamente implican un 50% y 50% de materia en cada lado de la reacción. Es simplemente un desplazamiento (determinado por la termodinámica), que favorece la formación de un compuesto antes de otro (o en mayor proporción).
También es importante aclarar que, aun cuando se denomina equilibrio, es un equilibrio dinámico, ya que la reacción sigue produciéndose (en ambas direcciones) solo que, ambas velocidades permiten que la concentración o presiones parciales de los compuestos permanezcan invariantes en el tiempo.
Variación del Número de Moles (∆n):
Sumatoria del número de moles de productos gaseosos, menos la sumatoria del número de moles de los reactantes gaseosos (Si se consediera un equilibrio entre gases, los compuestos en estado solido no intervienen en la constante de equilibrio).
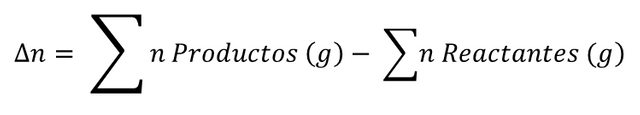
∆n=0→Kc=Kp
Relación entre Kc y Kp
Se define como Kc a la constante de equilibrio determinada por la relacion entre las concentraciones de los compuestos. Sin embargo tambien puede asociarse una constante de presion Kp, la cual considera la relacion entre las presiones parciales de cada componente.
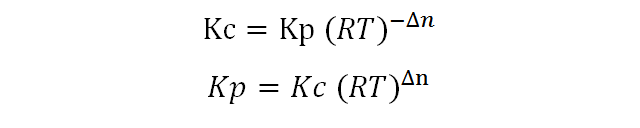
Si Kc > 1 → Mayor cantidad de productos con respecto a los reactantes.
Si Kc < 1 → Mayor cantidad de reaccionantes con respecto a los productos.
Valor de K Según la forma de la ecuación Balanceada
Es importante tener en cuenta que se debe balancear la ecuación siempre, antes de calcular el valor de la constante de equilibrio, ya que ésta involucra los coeficientes estequiométricos. Dada la siguiente reacción general:
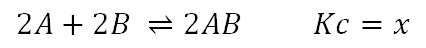
Entonces:
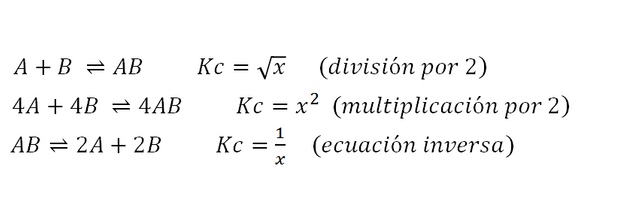
Predicción de la Dirección del Equilibrio:
Si se tienen condiciones iniciales de un proceso de equilibrio química (valores de concentraciones o presiones parciales) y se tiene la ecuación química balanceada junto con la constante de equilibrio, se puede calcular fácilmente la dirección que “tomará” el equilibrio luego de haber transcurrido un tiempo t. Para ello se emplea el calculo del coeficiente de reacción (Q), el cual matemáticamente tiene la misma forma que la constante de equilibrio, pero a diferencia de esta, se calcula con los valores iniciales, y su interpretación es diferente:
Q < K , Reacción neta Reactantes → Productos
Q > K , Reacción neta Productos → Reactantes
Q = K , Estado de equilibrio.
Grado de disociación y porcentaje de disociación:
Uno de los cálculos mas frecuentes cuando se estudian equilibrios químicos, es el grado y porcentaje de disociación. Esta ecuación nos permite obtener un valor que representa cuan gran es la parte disociada de un equilibrio según la cantidad inicial. Es una proporción que nos permite también interpolar a escenarios donde las cantidades de reactivos iniciales sean mayores o menores, y también entre otras reacciones similares. Por ejemplo podemos comparar que compuesto salino es mas soluble en etanol, con sus respectivos valores del grado o porcentaje de disociación.
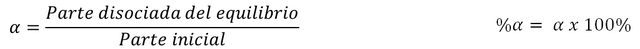
Cálculo de presiones y fracciones molar
A continuación, se presentan algunas formulas de interés, al momento de calcular constantes de equilibrio.
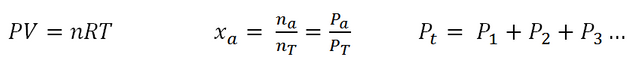
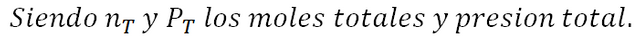
Principios de Le Châtelier
Adición o Sustracción de Reactantes o Productos:
Al adicionar reactantes a una ecuación en equilibrio, esta actuará de tal manera de consumir la cantidad de reactante necesaria para establecer de nuevo el equilibrio.
Al sustraer reactantes a una ecuación en equilibrio, esta actuará de tal manera de disociar la cantidad de productos necesaria para establecer de nuevo el equilibrio.
Es decir, las concentraciones so presiones parciales del equilibrio se desplazarán para lograr nuevamente el estado de equilibrio (Alcanzar nuevamente el valor de K)
Cambio de Presión por Variación de Volumen.
Cuando aumentamos el Volumen, disminuye la presión, el sistema comienza a aumentar los moles, entonces la reacción neta se produce desde donde hay menos moles hacia donde hay más moles, de esta forma, se alcanzan nuevamente los valores de presión, y se reestablece el estado equilibrio.
Cuando disminuimos el Volumen, aumenta la presión, el sistema comienza a aumentar los disminuir, entonces la reacción neta se produce desde donde hay más moles hacia donde hay menos moles.
Cuando ∆n=0 , los cambios de volumen no afectan la dirección del equilibrio, solo cambian las concentraciones o presiones parciales.
Adición de un Gas Inerte
Aumenta la Presión total y el número de moles totales, disminuye cada Fracción Molar de las especies. Las presiones parciales permanencen invariantes.
Cambio de Temperatura
∆H=Cambio de entalpia
Cuando ∆H>0 El sistema es endotérmico, al aumentar T , aumenta K, si disminuye T, disminuye K, el aumento de temperatura es directamente proporcional al valor de K. El sistema se favorece aumentando la temperatura.
Cuando ∆H < 0 El sistema es exotérmico, al aumentar T, disminuye K, si disminuye T, aumenta K, el aumento de temperatura es inversamente proporcional al valor de K. El sistema se favorece disminuyendo la temperatura.
Si invertimos el sentido de una reacción, ∆H cambia su signo matemático.
Adición de un Catalizador
La catálisis es el proceso por el cual se aumenta la velocidad de una reacción química, debido a la participación de una sustancia llamada catalizador. En este caso el equilibrio se alcanza más rápido debido a la accion del catalizador.

Espero que este artículo haya sido de su agrado,el equilibrio quimico esta presente en muchas areas y es tema vita de investigacion para el desarrollo de nuevos fármacos, procesos, materiales, etc. Personalmente considero muy importante conocer cada día más el mundo que nos rodea y las manifestaciones del mismo que, en gran medida, lograran sorprendernos.
Seguimos a la espera de los grandes desarrollos que nos traerá el futuro, tú decides si ser espectador o realizador. Todos los días podemos aprender algo nuevo.
Gracias por leer.
Referencias:
Todas las imágenes y sepradores de mi autoría, fueron editados y procesados utilizando el programa PowerPoint 2016.
- Theodore Brown, Eugene LeMay, Bruce Bursten, Julia Burdge, (2004), Quimica. La ciencia central. (9° Edición). Pearson Educación, S.A.
Douglas Skoog, Donald West y James Holler (2006) Fundamentos de Química Analítica (4ta Edición) Editorial Reverté.
CRC HandBook of Chemistry and Physics, 86th Edition, CRC Press 2005
Arthur I. Vogel et al. (1989) Textbook of Quantitative Chemical Analysis, 5th edition, Longman Scientific & Technical.

Posted from my blog with SteemPress : http://aleestra.vornix.blog/equilibrio-quimico-del-dinamismo-a-lo-constante/
Congratulations! This post has been upvoted from the communal account, @minnowsupport, by Aleestra from the Minnow Support Project. It's a witness project run by aggroed, ausbitbank, teamsteem, someguy123, neoxian, followbtcnews, and netuoso. The goal is to help Steemit grow by supporting Minnows. Please find us at the Peace, Abundance, and Liberty Network (PALnet) Discord Channel. It's a completely public and open space to all members of the Steemit community who voluntarily choose to be there.
If you would like to delegate to the Minnow Support Project you can do so by clicking on the following links: 50SP, 100SP, 250SP, 500SP, 1000SP, 5000SP.
Be sure to leave at least 50SP undelegated on your account.
Ciertamente es un tema muy estudiado en química y cuya verificación en el laboratorio es una de las experiencias que más atrae la atención de los estudiantes que se inician en el estudio de la química.
Jejeje si, y para hacer que un pescado deje de estar salado, irónicamente agregándole sal común. Gracias por comentar, saludos.
This post has been voted on by the steemstem curation team and voting trail.
There is more to SteemSTEM than just writing posts, check here for some more tips on being a community member. You can also join our discord here to get to know the rest of the community!
Hi @aleestra!
Your post was upvoted by utopian.io in cooperation with steemstem - supporting knowledge, innovation and technological advancement on the Steem Blockchain.
Contribute to Open Source with utopian.io
Learn how to contribute on our website and join the new open source economy.
Want to chat? Join the Utopian Community on Discord https://discord.gg/h52nFrV