Propiedades del agua. Parte II.
Saludos estimados amigos y lectores.
En una publicación anterior iniciamos la descripción de las propiedades del agua, en ese artículos nos enfocamos en describir las principales propiedades físicas que le dan sus particulares características a nuestro más apreciado líquido; pero el tema resultó algo extenso para una sola publicación, por eso hoy pretendo continuar su descripción ahondando en otras propiedades que son consecuencia de la interacción intermolecular entre sus moléculas y que le confieren algunos peculiares comportamientos, hablo de la tensión superficial y la capilaridad.

Fuente: imagen editada por el autor, original de wikimedia.com
¡Comencemos!
Tensión superficial
De alguna forma hemos sido testigos de esta particular propiedad que tienen los líquidos que se conoce como tensión superficial, quizás hayan visto como sobre la superficie del agua pueden posarse pequeños insectos sin hundirse, como se forman burbujas de aire o la forma de las gotas de agua sobre la superficie de materiales encerados o impermeables.

Fuente: pxhere.com
La tensión superficial es la capacidad que tiene un líquido de comportarse como una delgada película de elástica tensionada debido a las fuerzas de atracción entre las moléculas de que se encuentran sobre la superficie. En el seno del líquido las moléculas son jaladas en todas direcciones, por lo que las fuerzas intermoleculares se encuentran equilibradas; sin embargo, las moléculas que se encuentran en la superficie interactúan con las moléculas que tienen a los lados y por debajo, pero con ninguna en la parte superior, observen la siguiente figura:
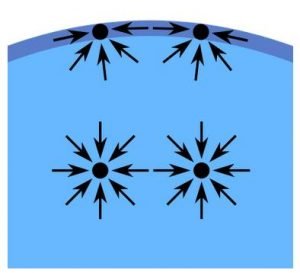
Fuente:wikipedia.com
Por ello, estas interacciones desiguales hacen que las moléculas en la superficie sean jaladas hacia el líquido, producto de una atracción neta hacia el interior del líquido, ocasionando que la superficie se tense como si se tratara de una película elástica, por lo que la superficie del agua se vuelve un poco más resistente a ser penetrada por un objeto extraño. Todos los líquidos presentan tensión superficial, pero mientras mayor sean las fuerzas de unión entre sus moléculas esta será más grande, y debido a que las fuerzas de unión producidas por los puentes de hidrógeno son más intensas, en el agua la tensión superficial es mayor que en la mayoría de los líquidos.
Otro ejemplo de la tensión superficial es la forma que adoptan las gotas de agua sobre una superficie impermeable. Como en el caso de las gotas de agua sobre la superficie cerosa de una hoja, dada la polaridad de las moléculas de agua esta tiene poca afinidad o atracción por moléculas no polares, por lo que más bien se repelen y las gotas de agua adquieren la forma de una pequeña esfera minimizando su área superficial.

Fuente: pxhere.com
Si deseamos cuantificar esta fuerza podemos considerar la siguiente estructura compuesta de un lado deslizante el cual se coloca una capa de agua en el interior.
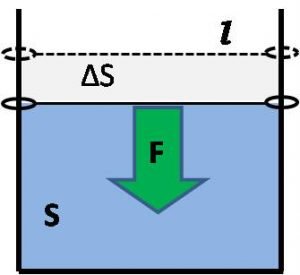
Fuente: elaboración propia.
El agua tratará de minimizar el área superficial S aplicando una fuerza F sobre el lado que se desliza, estableciéndose que:
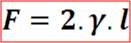
Donde γ es la tensión superficial del agua, y F depende de la longitud del lado deslizante (l). Esta fuerza F es perpendicular al lado deslizante y paralela a la superficie del líquido.
La tensión superficial también describe la energía por unidad de área requerida para estirar o aumentar la superficie de un líquido.
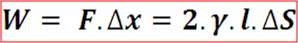
De ahí que la superficie de un lago sea plana o que las gotas de lluvia al caer tiendan a formar un volumen esférico.
La tensión superficial del agua no es un valor constante, se ve afectada por la temperatura o la adición de otra sustancia. En la siguiente tabla se muestran algunos valores de la tensión superficial para algunos líquidos.
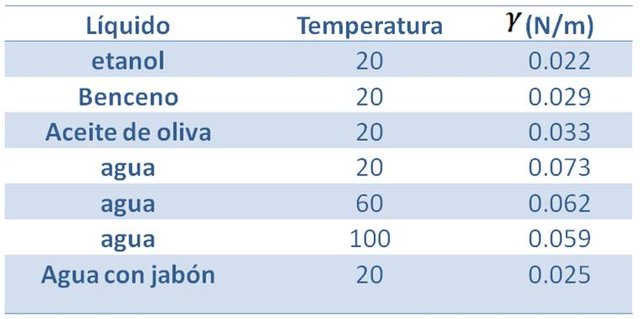
Como se puede observar en la tabla anterior, el agua presenta mayor tensión superficial que algunos líquidos, y la tensión superficial de la misma se puede modificar bien por la acción de la temperatura como por la adición de un surfactante. Reducir la tensión superficial es importante para facilitar que el agua moje, especialmente en el caso del lavado de ropa y utensilios, y también porque permite penetrar a través de irregularidades en tejidos, primordial para la aplicación de ciertas proteínas en los alveolos pulmonares.
Acción capilar
Otro ejemplo de la tensión superficial del agua es la capacidad que tiene esta de subir espontáneamente por un tubo capilar. En la siguiente imagen se describe el proceso.
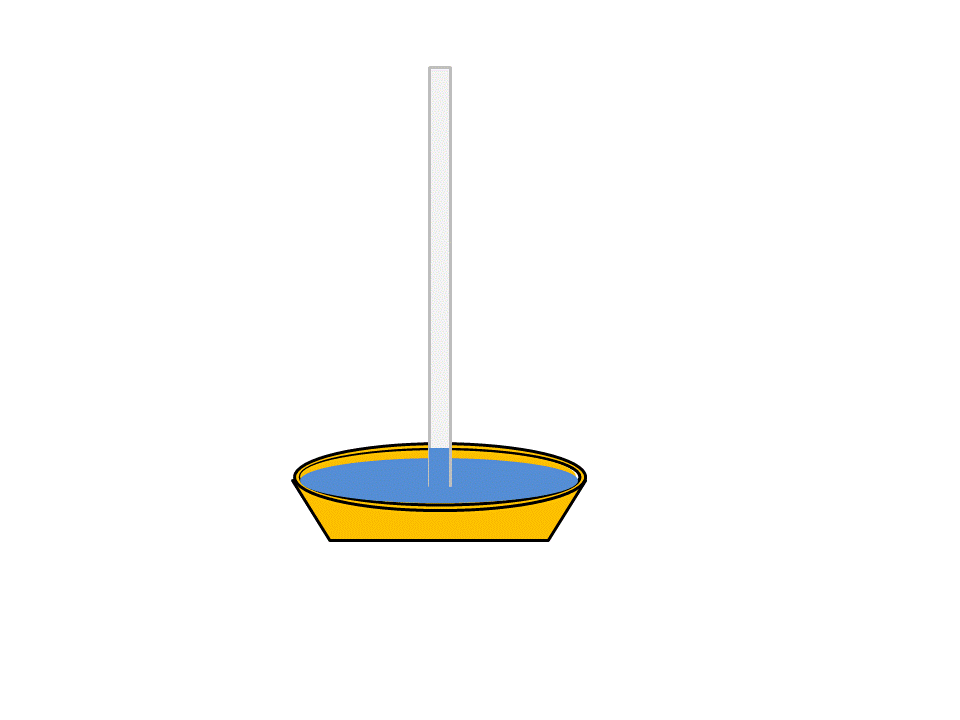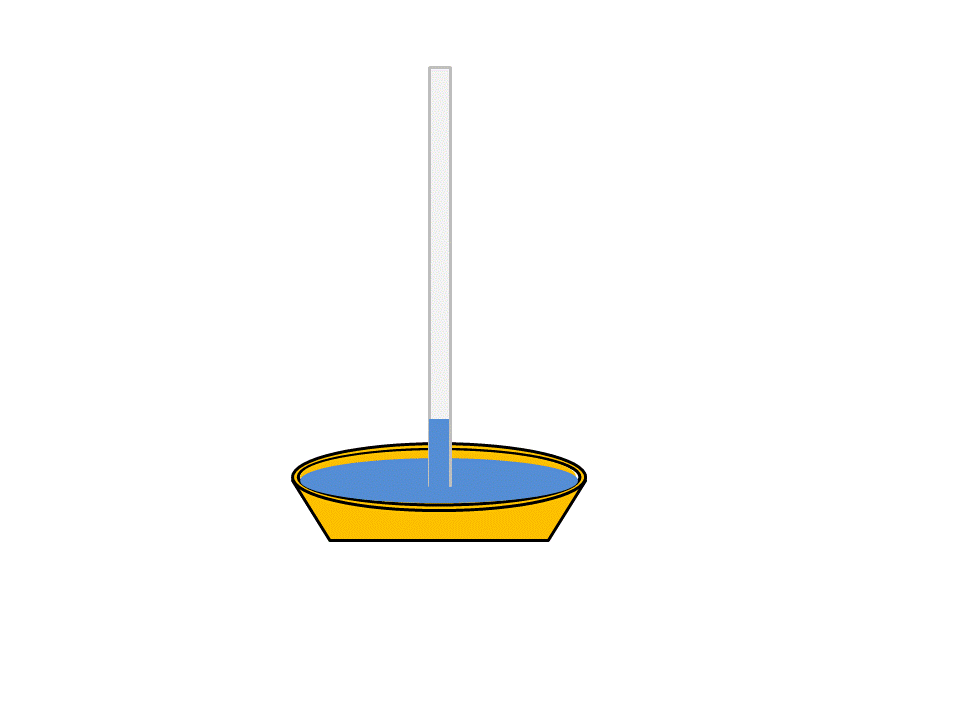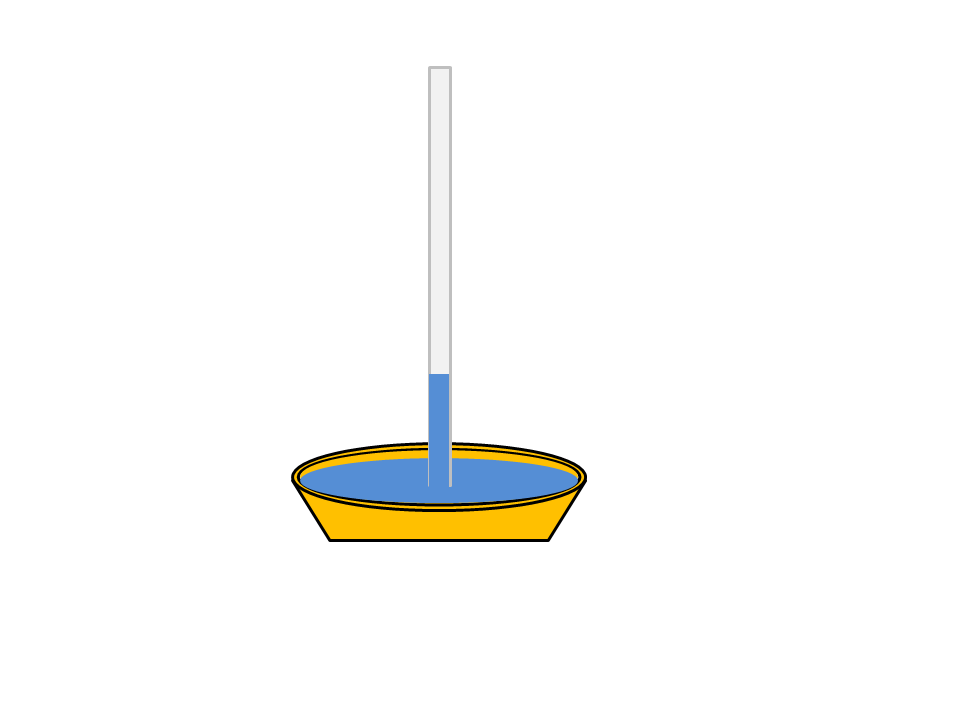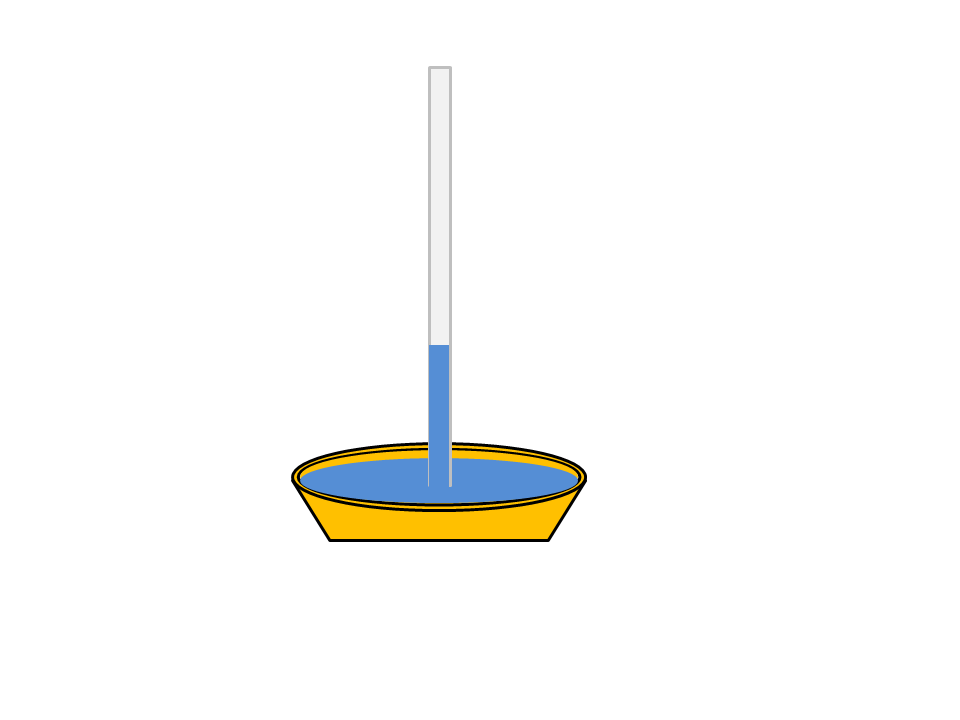
Fuente: elaboración propia.
Cuando la delgada película de agua de la superficie se adhiere a la superficie del tubo, la tensión superficial hace que esta película se contraiga, provocando que el líquido sea jalado hacia arriba en el interior del tubo. Esta propiedad del agua es producida por dos tipos de fuerzas: la cohesión y la adhesión.
La cohesión es la fuerza de atracción intermolecular entre moléculas semejantes, es decir, de las moléculas de agua por sí misma; por otro lado, la adhesión se refiere a la fuerza de atracción intermolecular entre moléculas diferentes, como en el caso del ejemplo, entre las moléculas de agua y el tubo de vidrio. Cuando la adhesión es más fuerte que la cohesión, las moléculas de agua tienden a mojar las paredes del tubo de vidrio, por lo que el contenido será impulsado hacia arriba.
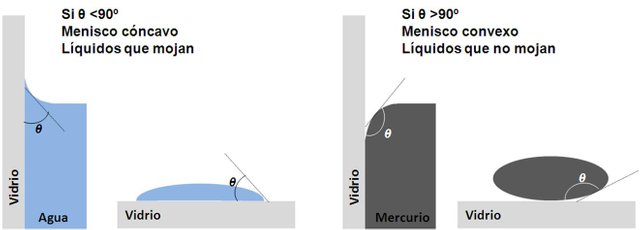
La relación entre ambas fuerzas determina la forma que adopta de la superficie del líquido que está en contacto con una pared sólida. Cuando las fuerzas de adhesión son las predominantes (en el caso del agua en contacto con el vidrio) se forma un menisco cóncavo, dado que el líquido tiende a extenderse sobre la superficie; en cambio, cuando las fuerzas de cohesión son las que predominan (ejemplo de ello el mercurio en contacto con vidrio) se forma una menisco convexo dado que el líquido tiende a mantenerse unido en lugar de extenderse por el material.

Referencias
Maron & Prutton. Fisicoquímica. editorial Limusa.
Fenómenos de superficie
Tensión superficial
Capilaridad
Posted from my blog with SteemPress : https://moronej.000webhostapp.com/2018/08/propiedades-del-agua-parte-ii
Me encanta la química y como la defiendes con tanta pasión.
Saludos Breili. Me alegra que te guste la química y especialmente que encuentres interesante el contenido de mi blog, aprecio que te tomes el tiempo de pasar por acá. Saludos!!!
Genial. Leyendo recordé muchas cosas de cuando vi este tema hace ya algún tiempo, fue uno de mis favoritos. Buena información, saludos @amiliomoron
Gracias estimado @fran.rey, el tema de las propiedades y características del agua también es de mis favoritos, me alegra que te gustara la información. Saludos!