[과학]얼음과 엔트로피

[사진 pixabay 참조]
더운날 집에 앉아 아이스크림을 먹으면서 얼마 지나지도 않았는데 아이스크림이 거의 다 녹아 흐느러지는 것을 보면서, 얼음이 녹는 과정에 대해서 생각해 보게 됬다.
얼음은 상온(27도, 300K)에서 녹는데 이 과정이 가역적인 반응일지 비가역적인 반응일지 ㅋㅋㅋ 물론 상온에서는 얼음이 얼지 못하니[상온에서 얼음이 언다면 머하러 냉장고를 산단 말인가!] 이 과정은 비가역적인 반응인게 자명하다.
하지만 계산, 증명을 좋아하는 나로써는 이 반응을 직접 계산해서 이론적으로 이 반응이 실제로 비가역적인 반응이다라는 것을 보이는게, 증명하는게 중요하다. [사실 생각해보면 일련의 과정은 열물리의 예제 정도로 적합한 사고과정이다, 아마 유사한 문제를 풀었던 기억으로 인해 이런 궁금증이 떠오른 것이 아닐까 싶다.]
가역과 비가역적 반응임을 살펴보기 위해서는 총 얼음과 얼음의 계의 총 엔트로피를 구해보면 알 수 있다. 이 총 엔트로피가 증가한다는 것은 해당 과정이 비가역이라는 것을 말해준다. [열역학 제 2법칙!!!]
자 그럼 모델링을 해보자. 얼음의 온도는 0도 (273K)로 100g 으로 가정하자. 얼음이 녹는 동안 얼음은 0도를 유지할 것이고 100g 에 해당되는 융해열은 33400J 이 된다. [ 잠열-위키 참조 ]
얼음이 받는 열과 대기가 받는 열의 량은 같을 것[얼음의 경우는 열을 받을 것이고 공기의 경우는 열을 방출 할 것이다. 이는 온도가 높은 쪽에서 온도가 낮은 쪽으로 열이 흐르기 때문이다: 온도의 정의] 이고 얼음은 0도를 (273K) 방안의 공기는 상온인 27도 (300K) 로 가정하자.
자 그러면 이제 얼음과 대기에 해당하는 엔트로피의 변화량을 구할 수 있다.
먼저 얼음
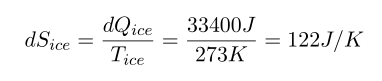
공기
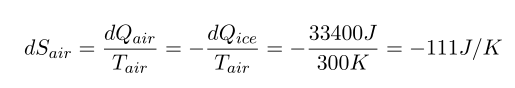
전체
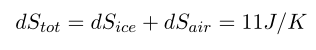
즉 전체 엔트로피가 증가하니, 이 과정이 비가역적 과정이라는 것을 알 수 있었다!
누군가는 다 아는 사실을 머하러 번거롭게 확인하느냐고 할 수 도 있다. 한번 쯤은 자기가 다 안다고 생각하는 것도 의심을 가져보고 확인해 보는 자세가 필요하다고 생각해 글을 남겨 본다.
때로는 누구나 다 아는 사실을 번거롭게 확인해보면 검증 과정을 통해 새로운 사실을 발견하게 될 수도 있지만 보다 근본적으로 알려진 정답이 왜 물리적으로 타당한 현상인지 가슴에 와닿게 되는 것 같습니다.